چگالي زياد را از دو طريق مي توان توضيح داد:
1- تغيير حالت فيزيكي: بدين ترتيب كه انقباض و تراكم مواد پوسته اي به حجم هاي بسيار كوچكتر تحت فشارهاي خيلي زياد باعث افزايش چگالي شود.
2- تغيير در تركيب شيميايي: كه طي آن افزايش چگالي بخاطر حضور بعضي از مواد باشد كه ماهيتاً سنگين تر باشند مانند فلزات سنگين.
يولن: توزيع چگالي درون زمين را كه با چگالي كل و ممان اينرسي آن جور در مي آيد محاسبه كرد.
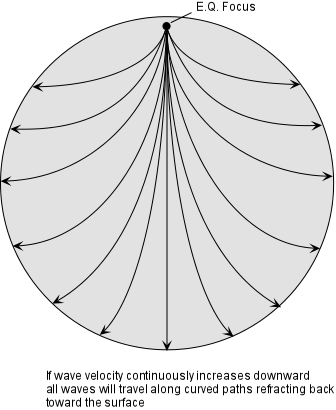
يولن از روي نتايج فوق توزيع فشار درون را محاسبه كرد. فشار درون زمين 3640 كيلوبار و يا به بيان ديگر بيش از 3 ميليون اتمسفر است. تحقيقات بعدي مشخص كرد كه منحني هاي تعميم يافته اي كه توسط يولن ترسيم شده اند ساختمان مشخص مهمي را بخصوص در گوشته فوقاني نشان مي دهد كه در تصوير زير آمده است.
![]()
![]()
دماهاي درون زمين
فشار در زير سنگ كره در هر نقطه با توجه به ضخامت و چگالي سنگهاي فوقاني تعيين مي شود فشار را بعنوان تابعي از عمق زمين محاسبه مي كنند. فشار در مركز زمين بيش از 5/3 ميليون برابر فشار اتمسفر سطح زمين است.
دما: اندازه گيري دما كار ساده اي نيست.
شيب گرمايي (Thermal gradian) : در محدوده پوسته زمين بين 10 تا 50 درجه سانتيگراد در هر كيلومتر مي باشد كه ميانگين آن برابر 30 درجه سانتيگراد در هر كيلومتر است.
از روي شيب گرمايي و رسانايي گرمايي سنگها جريان حرارت به سطح زمين را مي توان محاسبه كرد.
ميانگين مقدار جريان حرارتي برابر 106×5/1 كالري بر سانتيمتر مربع بر ثانيه است.
مقدار سالانه برابر 50 كالري بر سانتيمتر مربع 1.5×10 cal/cm2/oc-6 كه براي ذوب يك صفحه يخ به ضخامت 6 ميليمتر كافي مي باشد. گرماي نهان ذوب يخ 80 كالري بر گرم است.
طبق مطالعات انجام شده: ميانگين جريان حرارتي اقيانوسي تقريباً برابر ميانگين جريان حرارتي قاره اي است.
منشأ حرارت قاره = حضور عناصر راديواكتيو در پوسته قاره اي. در حاليكه پوسته اقيانوسي نازك بوده و راديواكتيو كمتري داشته است و توانايي توليد بيش از ده درصد از جريان حرارتي اقيانوسي را ندارد.
منابع تعيين حرارت:
1-30 تا 50 درصد از جريان حرارتي قاره ها ( از سنگهاي پوسته تأمين مي شود)
2- باقيمانده جريان حرارتي قاره اي و اقيانوسي (گرماي عمقي درون زمين است Deep Heatشدت جريان حرارتي به شرح زير است
(Ocean Trenches) < (Ocean Basines) < (Ocean Ridges)
بخش مهمي از گرماي بستر اقيانوسي از طريق سلولهاي همرفتي بزرگ جبه كه در فرآيندهاي تكتونيكي نقش دارند به سطح آورده مي شود. اين سلولها كه در تيغه هاي اقيانوسي به سطح مي رسند جريانهاي حرارتي بالا مشاهده شده را توليد مي كنند. فرو افتادن بستر اقيانوسي در مناطق دور از تيغه هاي در اثر سرد شدن و انقباض پوسته اي بستر اقيانوسي مي باشد.
دما جبه:
به استثناي بعضي از قسمتهاي سست كره، سرتاسر جبه جامد است. دما در قاعده جبه نمي تواند بيش از 10000 درجه سانتيگراد باشد. نقطه ذوب مواد واقع در قاعده جبه چيزي در حدود 4000 درجه سانتيگراد است. اين تخمين با حضور هسته اي متشكل از آهن مذاب جور در مي آيد.
تغييرات نقطه ذوب با فشار براي ديوپسيد 10 درجه در هر كيلوبار و يا به بيان ديگر 3 درجه در هر كيلومتر تعيين گرديده است.
ساختمان دروني زمين:
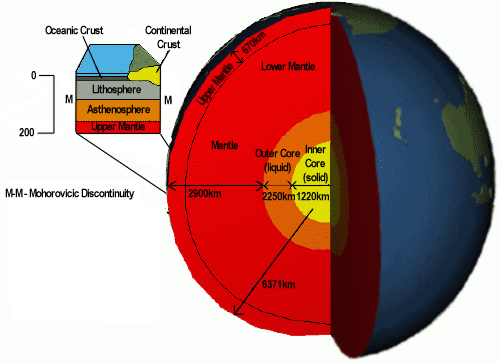
با توجه به داده هاي لرزه نگاري ساختمان دروني زمين به سه بخش اصلي تقسيم شده اند كه از بالا به پائين عبارتند از : پوسته گوشته و هسته.
ب) پوسته:
ناهمگن با ضخامت متفاوت. ناپيوستگي موهوروويچيك در محيط هاي مختلف زمين در اعماق مختلف يافت مي شود.
ناپيوستگي موهو در پوسته اقيانوسي 10 تا 13 كيلومتر و در زير پوسته قاره اي 35 كيلومتر تا زير سطح دريا بوده و در زير كمربند هاي كوهستاني فعال به اعماق معمولاً بيشتر از 60 كيلومتر مي رسد.
وضعيت اقيانوسها: بررسيها نشان مي دهد كه عمق آب دريا حدود 4 كيلومتر، در زير آب تا 2 كيلومتر رسوبات سست، در زير رسوبات نيز موادي با تركيبات بازالتي 5 تا 8 كيلومتر تا ناپيوستگي موهوروويچيك گسترده شده است.
انفصالات يا ناپيوستگي در درون زمين:
مسير امواج دروني در كره زمين نيز بطور كلي منحني شكل است. در جائي كه سنگهائي با خصوصيات فيزيكي كاملاً متفاوت در كنار هم قرار گرفته باشند سرعت امواج لرزه اي ناگهان تغيير مي كند و در نتيجه مسير امواج شكستگي مشخص را نشان مي دهد. چنين مرزهايي را در داخل زمين انفصال يا ناپيوستگي گويند.
در نتيجه زمين به سه بخش پوسته گوشته و هسته تقسيم شده است.
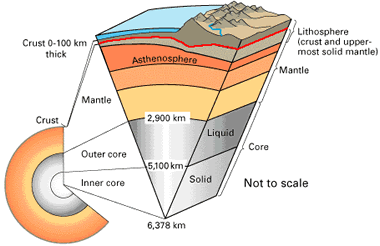
مرز پوسته و گوشته (موهو) (Mohorovicic) :
انفصال موهوروويچ يا بطور خلاصه موهو كه با افزايش سرعت هاي امواج مشخص مي شود سرعت بيشتر امواج لرزه در گوشته و پديده انكسار و موج انتقال اندازه گيري ضخامت پوسته را فراهم مي كند.
دو عامل مهم:
اختلاف زماني رسيدن امواجي كه بخشي از مسير خود را در گوشته طي مي كنند و امواجي كه مسير آنها مستقيماً در پوسته است به دو عامل بستگي دارد:
سرعتهاي نسبي امواج لرزه اي در گوشته و پوسته
1- ضخامت پوسته
خصوصيات پوسته:
خارجي ترين قسمت سطح ليتوسفر را پوسته گويند و بطور متوسط داراي 35 كيلومتر ضخامت مي باشد. در بعضي جاها به 50 الي 60 كيلومتر نيز مي رسد.
پوسته اقيانوسي برابر 10 تا 12 كيلومتر مي باشد و شامل بازالت و گابرو است. (خواص الاستيكي)
پوسته قاره اي برابر 20 الي 60 كيلومتر مي باشد و شامل گرانيت و ديوريت است. (خواص الاستيكي)
پوسته موزائيكي متشكل از رسوبات رسوبات دگرگوني انواع نفوذي هاي آذرين دروني و بيروني كه بصورت قطعات با اندازه و شكل هاي مختلف گسليده و شكسته شده است.
پوسته قاره اي از دو قسمت ساخته شده است:
1- پوسته فوقاني يا سيال (Sial) : عمدتاً از سيليكات و آلومينيم تشكيل شده است. به علت وجود سنگهاي اسيدي و گرانيتي به آن پوسته گرانيتي نيز گفته مي شود. ضخامت 15 تا 20 كيلومتر انفصال كونراد . (Conrad Discotiouty)
2- پوسته تحتاني يا سيما (Sima) : عمدتاً از سنگهاي بازيكي شبيه گابرو و بازالت تشكيل شده است. ضخامت 15 كيلومتر و سرعت امواج P برابر 6 تا 7 كيلومتر بر ثانيه است.
شكل----: لايه هاي مختالف پوسته را نشان ميدهد
الف) گوشته:
داده هاي ژئوفيزيكي نشان مي دهد كه جبه داراي ساختار لايه اي است. گوشته بعد از پوسته شروع مي شود و تا عمق 2900 كيلومتر از سطح زمين ادامه دارد. با انفصال موهو گوشته از پوسته جدا مي شود. تعيين مواد سازنده جبه عمدتاً بر مبناي ميانبارها است.
گوشته به سه قسمت تقسيم مي شود:
الف) گوشته فوقاني (Upper Mantle) : از زير پوسته شروع و تا 413 كيلومتري ادامه دارد.
انواع سنگهاي جبه – سه نوع سنگ وجود دارد: 1- دونيت (اليوين) 2- پريدوتيت (اليوين + پيروكسن) 3- اكلوژيت (گارنت و پيروكسن)
ب) گوشته مياني يا ناحيه گذر (Transition Zone) : از 413 تا 984 كيلومتري.
منشأ: ماگماها، شروع زمين لرزه عميق، تكتونيك جهاني و شناوري قاره اي در جبه بالا و منطقه مياني نهفته است.
ج) گوشته زيرين (Lower Mantle) : از 984 تا 2900 كيلومتري. تركيبات آن شامل روتيل، اسپينل و سولفورها – جامد. وزن مخصوص آن 5 تا 5/4 مي باشد.
سرعت موج P برابر 8 كيلومتر بر ثانيه است.
تعيين مواد سازنده جبه عمدتاً بر مبناي نمونه هاي احتمالي مواد جبه قرار دارد كه بصورت ميانبار در لوله هاي آتشفشاني ديده مي شود.
1 – 2- گوشته يا جبه بالائي
مواد تشكيل دهنده جبه بالائي (Upper Mantle) :
1- سنگ دونيت (اليوين)
2- پريدوتيت (اليوين و پيروكسن)
3- اكلوژيت (گارنت و پيروكسن)
عمدتاً سيليكاتها Fe و Mg، ميانبارهاي پريدوتيتي و دونيتي گاهي اوقات در سنگهاي آتشفشاني به فراواني يافت مي شود.
منشأ ماگماي بازالتي هاوائي حدود 60 كيلومتر مي باشد.
وجود الماس در كيمبرليت دلالت بر منشأ عميق تر يعني بيش از 100 كيلومتر است.
ماهيت يا علت ناپيوستگي موهوروويچيك:
دو طرز تفكر براي ناپيوستگي پوسته و گوشته وجود دارد.
1- تغييرات فيزيكي: تبديل سنگهاي پوسته پائيني يا تركيب گابروي به اكلوژيت كه ماده چگال تر است اما با همان تركيب.
2- ناپيوستگي شيميايي: جبه بالائي را يك تركيب اولترابازيك (دونيت يا پريدوتيت) در نظر مي گيرند.
3- رينگ وود (1975) : اطلاعات پترولوژيكي، ژئوفيزيكي و ژئوشيميايي را با يكديگر تطبيق كرد و يك مدل اولترابازيكي را براي جبه پيشنهاد داد. كه عبارت است از محلي از يك قسمت بازالت و سه قسمت دونيت كه اين تركيب را او پيروليت (Pyrolite) ناميد كه يك سنگ پيروكسن اليوين دار مي باشد.
3دونيت + بازالت = پيروليت
ذوب بخشي پيروليت: ماگما را توليد مي كند. لذا مينرالوژي پيروليت تابعي از دما و فشار است. رينگ وود نشان داد كه موادي با اين تركيب به صورت چهار مجموعه مشخص به شرح زير متبلور مي شود.
Olivin + Ampholite 1- آمفوليت
Olivine + Al-Poor Pyroxene + Plagioclase 2- پيروليت پلاژيوكلاز دار
Olivine + Al -Poor Pyroxene + Spinel 3- پيروليت پيروکسن دار
Olivine + Al -Poor Pyroxene + Garnet 4- پيروليت گارنت
از آنجا كه ژئوترم هاي گوشته فوقاني زير قاره اي و اقيانوسي ميزان قابل توجهي با هم تفاوت دارند. تفاوت ناحيه اي در تركيب كاني شناسي پيروليت وجود دارد. تركيب استنباطي گوشته فوقاني در زير سپر پركامبرين مناطق ميانگين قاره اي و اقيانوسي در شكل نشان داده شده است. بعلت اختلاف خطوط زمين گرمائي در جبه بالائي تفاوت منطقه اي در تركيب كانيهاي پيروليت وجود دارد.
جبه بالائي در زير سپر پركامبرين
1- ميانگين مناطق قاره اي
2- ميانگين مناطق اقيانوسي
2 – 2 – گوشته مياني يا منطقه گذر: TRANSITION ZONE
اهميت جبه مياني: The Important Of Transition Zone
1- درك اهميت تغييرات پلي مورفيك (Polymorphic Changes) در دما و فشار بالا نقش بسزايي در توسعه اطلاعات از ناحيه مياني جبه داشته است.
برنال (1936) (Bernal) : ناپيوستگي بين جبه بالايي و منطقه مياني را ناشي از تشكيل يك پلي مورف فشار بالاي اليوين مي داند كه به دو صورت وجود دارد:
ساختار اليوين MgGeSiO4
ساختار اسپينل (Mg,Fe)2SiO4 كه ساختار اسپينل 9% چگال تر از اليوين است.
استيشف (Stishov) و پوپوآ (Popova) (1961) : اين دو دانشمند شكل روتيلي SiO2 ساخته و استيشوويت (Stishovite) نام گرفت. خواص فيزيكي استيشوويت در 130 كيلوبار 1600 درجه سانتيگراد پايدار است.
پيشنهادات كلارك و رينگ وود در مورد پلي مورفهاي جبه مياني:
اين دو نفر داده هاي پلي مورفيك را براي استنتاج تركيب منطقه مياني جبه بكار گرفتند.
بنا به اعتقاد آنها اين منطقه عمدتاً از MgO و SiO2 كه با مخلوطي از اليوين Mg2SiO4 و پيروكسن MgSiO3 مطابقت مي كند تشكيل يافته است. اين فازها تا عمق حدود 400 كيلومتري پايدار هستند. در زير اين عمق يك سري تغيير شكل به فازهاي داراي بسته بندي فشرده تر صورت مي گيرد. اين دو محقق بر مبناي داده هاي موجود فرض كردند كه با افزايش عمق تغييرات زير رخ مي دهد:
اسپينل Mg2SiO4 Mg2SiO4 (Pyroxen)
استيشوئيت Mg2SiO4(Oli) + Si2 2MgSiO4(Pyroxen)
ايلمنيت +SiO2 (Stishovite) = 2MgSiO3 (اسپينل) Mg2SiO4
پريكلاز = MgSiO2 (Illminite) + MgO (اسپينل) MgSiO3
اين رشته تغيير شكل در عمق حدود 1000 كيلومتر كامل شده و در نتيجه چگالي از 2/3 به 9/3 افزايش مي يابد. عناصر اضافي مانند Ca ,Al ,Na ,Fe كه بصورت جايگزيني اتمي فازهاي اصلي حضور دارند. اين عناصر بر تبادلات تأثير مي گذارند و باعث ايجاد يك افزايش چگالي پيوسته بجاي افزايش پلكاني (Stepwise Inerease) مي شود.
جبه پاييني(LOWER MANTEL) :
از عمق 1000 تا 2900 كيلومتر قرار دارد به لحاظ تركيب شيميايي همگن بوده.
همگن = مخلوطي از (Mg,Fe)SiO3 با ساختار ايليمينيت و پريكلاز (Mg,Fe)O
رينگ وود: ساختاري با بسته بندي فشرده تر نيز مي تواند در جبه پائيني حضور داشته باشد.
هسته (سيدروسفر) (CORE) :
خواص فيزيكي هسته ايجاب مي كند كه هسته از عناصر واسطه تشكيل شده باشد.
طبق نظر جفري: دقت عمل اندازه گيري بين جبه و هسته برابر با 5/2 +- كيلومتر است. عبور امواج S از درون هسته مشاهده نشده است. اين امر بيانگر مايع بودن هسته حداقل در بخش بيروني است. منشأ احتمالي ميدان مغناطيسي زمين و تغييرات ديرپاي آن را مي توان از روي خود هسته آهني مايع استنتاج كرد.
الساسر(Elsaser) : طبق نظريه الساسر منشأ احتمالي ميدان مغناطيسي زمين و تغييرات ديرپاي آن را مي توان از روي خود هسته آهني مايع استنتاج كرد.
ميدان مغناطيسي زمين از جريانهاي الكتريكي درون آن ناشي شده است. تغييرات ديرپاي ميدان ژئومغناطيسي را در اين صورت مي توان به عنوان نمودي از جريانهاي همرفتي هسته اي مايع دانست.
ساختمان منطقه اي زمين: (Rigional Structure Of The Earth)
1- هسته آهني 2-جبه سيليكاتي نسبتاً همگن و داراي لايه بندي
2- پوسته سيليكاتي ناهمگن
اين تصوير از ساختار دروني زمين و تركيب شيميايي آن با جرم آن و ممان اينرسي آن و حضور ناپيوستگي مشخص شده بوسيله امواج لرزه اي همساز است. كاهش مقدار سيليس در توالي مواد كه از پوسته تا جبه قرار گرفته اند (با تجربيات پترولوژيكي هماهنگ مي باشد). تركيب احتمالي چنين زميني با وفور نسبي عناصر نيز سازگار است. براي كامل شدن اين تصوير ما بايد به پوسته جبه و هسته سه منطقه ديگر اضافه كنيم كه عبارتند از هواكره، آب كره و زيست كره.
اتمسفر هيدروسفر و بيوسفر = 3 % از كل جرم زمين را شامل مي شوند. پوسته كمتر از 1 % از جرم كل زمين را مي سازد. بنابراين تركيب كلي زمين عمدتاً از روي تركيب جبه و هسته تعيين مي شود ولي با توجه به اهميت پوسته در اينجا مورد بررسي قرار مي گيرد.
تركيب شيميايي پوسته زمين:
تركيب متوسط پوسته عملاً همان تركيب سنگهاي آذرين است.
كلارك و واشنگتن (1924): بطور تخمين اعلام داشته اند كه تا عمق 10 مايل پوسته عبارتند از :
95/0 % سنگهاي آذرين و دگرگوني، 04/0 % شيل، 75/0 % ماسه سنگ و 25/0 % سنگ آهك.
كار كلارك و واشنگتن نتيجه 5159 تجزيه كامل شيميايي بود.
طبق مطالعات كلارك و واشنگتن: درصد سيليس در سنگهاي نواحي اقيانوسي مانند جزاير اقيانوسي هاي اطلس و آرام به نحو قابل ملاحظه اي كمتر است و اين دليل ديگري است بر اين نظريه كه لايه سيال در زير اقيانوس نازك و يا وجود ندارد. ميانگين مجموع 5159 تجزيه شيميايي كه مجدداً نسبت به 100 محاسبه شده است با حذف H2O و اجزاي فرعي تشكيل دهنده آن بشرح زير است:
3/0=P2O5 06/1= TiO2 91/3 = Na2O 17/5 = CaO 56/3 = MgO 88/3 = FeO 14/3 = Fe2O3 61/15 = Al2O3 18/60 = SiO2
ايرادهاي وارده بر روش كلارك و واشنگتن:
1- توزيع جغرافيايي نابرابر نمونه هاي تجزيه شده.
2- توزيع غير آماري در انواع مختلف سنگي
3- عدم رعايت مقادير واقعي سنگهايي كه جهت تجزيه نمونه برداري شده است.
تأييد جالبي از اعتبار كلي ارقام بدست آمده توسط كلارك و واشنگتن بوسيله گلدشميت به عمل آمده است:
بنا به اعتقاد گلدشميت: رسوبات يخچالي جنوب نروژ نمونه هاي ريزدانه ترين پودر سنگي اند كه توسط آب ناشي از ذوب صفحات يخي فنواسكانديناويا رسوب يافته اند. نمونه هاي تهيه شده از اين رسوبات مي توانند معرف نمونه سنگهاي پوسته زمين باشند. از 77 نمونه تجزيه شده از نمونه هاي مختلف اين مواد متوسط آناليز زير را بدست مي آورد:
SiO2=59.12 , Al2O3=15.82 , Fe2O3=6.99 , MgO=3.30 , CaO=3.07 , Na2O=2.05 , K2O=3.93 , H2O=3.02 , TiO2=0.79 , P2O5=15.82
دانشمندان انستيتو ژئوشيمي ورنادسكي در مسكو با تجزيه چند هزار نمونه هاي متوسط سنگها از پلتفرم روسيه و ژئوسنكينال كوكازيان .... مطالعه سيستماتيكي را درباره پوسته زمين بعمل آوردند. طبق مطالعات فوق سه نوع پوسته تشخيص دادند:
1- پوسته قاره اي
2- پوسته اقيانوسي
3- پوسته زير قاره اي (اساسا منطقه حد واسط فلات و شيب قاره)
كه هر يک از اين پوسته ها در بردارنده لايه هايي از سنگهاي رسوبي و آذرين است. ميانگين ضخامت جرم و متوسط تركيب شيميايي هر يك از اين لايه ها تعيين و سپس با تلفيق آنها ميانگين هر يك ازنوع پوسته تعيين گرديد.
تعيين فراواني عناصر جزئي:
تعيين مقدار عناصر جزئي مسئله مشكل تري است. با اين وجود ظرف چهل سال گذشته بعلت .وارد شدن روشهاي تجزيه اي جديد مانند:
تجزيه طيف نگاري كمي (Quantitaive Spectrographic Analisis)
اندازه گيري هاي كالريمتري (Colorometric Determination)
فعال سازي نوتروني (Neotrian Activation)
طيف سنجي جذب (Atomic Absaption)
فلورسانس اشعه X (X Ray Flaorescance)
رقيق سازي ايزوتوپي (Isotope Dilation)
شيوه هاي مشخص كردن فراواني عناصر جزئي:
براي مشخص كردن فراواني عناصر فرعي و جزئي سه شيوه عمل مشخص بكار گرفته شده است:
1- تعيين ميانگين تعداد زيادي تجزيه مجزا
2- تجزيه مخلوطي از انواع سنگ
3- تعيين نسبت عنصر جزئي بعضي از عناصر رايج تر كه از نظر ژئوشيميايي با آنها همراه است مانند
اشاره به نقش استاندارد در آناليز:
براي اندازه گيري عناصر فرعي و كمياب اغلب از ارقام تبلور (1964) استفاده مي گردد كه ميانگين ها گرانيت ها و بازالتها را به نسبتهاي 1:1 تركيب مي نمايند
.گرانيت استاندارد 1-G از گرانيتي در وسترلي واقع در رود آيلند بدست مي آيد
و دياباز استاندارد 1-W ديابازي از سنترويل در ويرجينيا اساساً در حدود سال 1948 از دو سنگ فوق بدست آمده اند و داراي اين ويژگي هستند كه از گسترده ترين سنگهاي تجزيه شده در دنيا مي باشند.
اين دوسنگ بيشترين تجزيه شيميايي در جهان روي آنها انجام گرفته است و بخصوص عناصر فرعي و كمياب يا تكنيك هاي بسيار متنوع در آنها توسط آزمايشگاههاي تمام بخشهاي دنيا جهت تعيين مشکل اصلي انسان مورد تجزيه و تحليل قرار گرفته اند اين سنگها به عنوان استاندارد هاي ژئوشيميايي بكار گرفته شده اند.
فراواني عناصر جزئي بر اساس مطالعات 1-G و 1-W
داده هاي 1-G و 1-W همچنين نشان مي دهد كه عناصري مانند Be , Rb , Ba در گرانيت غني هستند و B , Sc , Ni در دياباز غني مي باشند. در حاليكه فراواني بعضي از عناصر مانند Zn , Ga , Ge در هر دو سنگ يكنواخت است. هشت عنصر O,Fi,Al,Fe,Ca,Na,K,Mg,Si تقريباً 99 % از فراواني كل را به خود اختصاص داده اند. از اين ميان اكسيژن مطلقاً بر ديگر عناصر فزوني دارد.
بنا به اعتقاد گلدشميت تمام پوسته زمين تقريباً از تركيب اكسيژن بويژه سيليكاتهاي آلومينيم، كلسيم، منيزيم، سديم، پتاسيم و آهن است. بر حسب تعداد اتمها اكسيژن تشكيل يافته است. بنابراين پوسته زمين اساساً يك بسته بندي از آنيونهاي اكسيژن است كه بوسيله سيليسيم و يون فلزات رايج به هم بسته شده است. همانطوريكه گلدشميت اظهار داشته است ليتوسفر را مي توان اكسي اسفر(Oxysphere) نام نهاد. اكسيژن بيش از 90 % حجم كل اشغال شده توسط عناصر را به خود اختصاص داده است.
عناصر پراكنده يا عناصر كمياب (Disperrese Elements Or Rare Element) :
عناصر كمياب در واقع همان عناصر پراكنده نيز مي باشند كه نقش بسيار مهم در حيات اقتصادي ما ايفا كرده اند. براي نمونه: فراواني مس بسيار كمتر از زيركونيم است. فراواني سرب با گاليم قابل مقايسه است. جيوه از تمام عناصر نادر خاكي كمياب تر است. روبيديم در مقاديري قابل ملاحظه با نيكل يافت مي شود. واناديم از قلع بسيار فراوانتر است. اسكانديم بسيار فراوان تر از آرسنيك و هافنيم بسيار فراوانتر از يد مي باشد.
برخي از عناصر اگرچه در پوسته در مقادير قابل توجهي حضور دارند اما بطور سيستماتيك در كانيهاي رايج پخش بوده و هرگز بصورت مجتمع رخ نمي دهند. ورنادسكي اين عناصر را عناصر پراكنده ناميد. مثال: روبيديم كه در كانيهاي پتاسيم و گاليوم كه در كانيهاي آلومينيم پراكنده است اشاره نمود. برخي عناصر مانند تيتانيم و زيركونيم كه كانيهاي خاصي را تشكيل مي دهند نيز به نوبه خود در مقادير بسيار اندك در رايجترين سنگها بصورت پراكنده ديده مي شوند.
توجه: بايد فراواني هر عنصر و در دسترس بودن آن را تميز قائل شد.
تعريف كلارك: فرسمن اولين كسي بود كه واژه كلارك را معرفي نمود. بر حسب تعريف وي كلارك درصد ميانگين يك عنصر در پوسته زمين است. مثال اكسيژن 60/46 و سيليسيم 72/27 .
كلارك غلظت: اين واژه توسط ورنادسكي معرفي شد. كلارك غلظت ضريبي است كه غلظت يك عنصر در يك رسوب خاص و يا حتي يك كاني بخصوص را نشان مي دهد. بدين ترتيب اگر كلارك Mn ،1% باشد كلارك غلظت منگنز در كاني پيرولوزيت 632 و در رودونيت 419 و در پسيلوملان 50 % يا 500Mn است. اين ضريب در ملاحظات مربوط به مهاجرت و رسوبگذاري عناصر و در مباحث مربوط به كانسارها مفيد واقع مي شود.
اگر كلارك منگنز 1% باشد. كلارك تمركز آن در پيرولوزيت 632 و كلارك تمركز آن در رودونيت 419 و در پسيلوملان با 50 % منگنز 500 است اين ضرايب در ملاحظات مربوط به مهاجرت و رسوبگذاري عناصر در مباحث مربوط به كانسارها مفيد واقع مي شود.
كانسنگ: هر كانسنگ را بسادگي مي توان بصورت رسوبي تعريف كرد كه در آن كلارك غلظت عنصر مورد نظر به عددي مي رسد كه استخراج آن را از نظر اقتصادي مقرون به صرفه مي كند.
عناصر قابل دسترس: قابل دسترس بودن يك عنصر تا حد زيادي به توانائي آن براي تشكيل كاني هايي بستگي دارد كه در آنها خود يك سازنده اصلي است.
غير قابل دسترس ترين عناصر:
آنهائي هستند كه كاني خاص خود را نمي سازند بلكه به مقادير بسيار كمتر از 1 % در كاني هاي عناصر ديگر يافت مي شوند. Ha,Ga,Rb و غيره از اين دسته اند.
جدول 7-3 برآورد كلارك هاي غلظت مورد نياز براي تشكيل توده هاي معدني فلزات رايج تر را نشان مي دهد.
|
کلارک غلظت لازم براي تشکيل يک توده معدني |
حداقل درصد استخراج سودآور |
کلارک |
فلز |
|
4 |
30 |
8.13 |
Al |
|
6 |
30 |
5.00 |
Fe |
|
350 |
35 |
0.10 |
Mn |
|
3000 |
30 |
0.01 |
Cr |
|
160 |
1 |
0.006 |
Cu |
|
125 |
1.5 |
0.008 |
Ni |
|
600 |
4 |
0.007 |
Zn |
|
5000 |
1 |
0.0002 |
Sn |
|
3000 |
4 |
0.0013 |
Pb |
|
500 |
0.1 |
0.0002 |
U |
سهل الوصول بودن عناصر:
استخراج Al از بوكسيت، استخراج منيزيم از آب دريا به ميزان 13 % در حالي كه رسوبات گسترده اي از اليوين حدود 30 % منيزيم دارد. محصول جانبي پروسه هاي استخراج به گونه اي نسبتاً آسان توليد مي شوند. مثال: پالايش الكتروليتيك مس مي تواند موجب توليد تلوريم به ميزان كافي جهت تشويق توسعه استفاده صنعتي از اين عنصر شود. گلدشميت خاطر نشان ساخت چنانچه تقاضايي براي گاليم و ژرمانيوم باشد. مقادير قابل ملاحظه اي از اين عنصر را مي توان از خاكستر برخي زغال ها استخراج كرد.
تفريق اوليه عناصر
بنظر مي رسد که زمين احتمالاً در اثر تجمع تدريجي سيارک هاي جامد تشکيل شده است. در واقع شخانه هاي کندريتي احتمالاً بخشهايي از سيارک هاي باقي مانده از مرحله پيش سياره اي در منظومه شمسي هستند. شخانه هاي کندريتي از سه فاز يا سه گروه مختلف تشکيل يافته اند که عبارتند از : نيکل – آهن ، سولفيد – آهن ، کانيهاي سيليکاتي (عمدتاً اليوين و پيروکسن). عناصر بر حسب آفينيته نسبيشان به فلز ، سولفيد ، يا سيليکات بين اين فازها توزيع شده اند. توزيع اين فازها در شخانه ها اصولاً از روي شرائط تعادل سيستم Fe - Mg- Si – O – S تعيين مي شود که در آن مقدار اکسيژن به مراتب بيش از سولفور و مجموع اين دو نيز به حدي نبوده که بتواند بطور کامل با عناصر الکتروپوزيتيو ترکيب شود. از آنجا که آهن فراوانتراز Mg , Si بوده به آساني به صورت فلز آزاد احيا شده و با داشتن بيشترين آفينيته براي گوگرد سيستمي متشکل از سه فاز ناميژاک تشکيل شد که عبارت بود از سيليکات آهن و منيزيم ، سولفيد آهن، و آهن آزاد. مقدار آهن ترکيب شده از روي مقادير اکسيژن و گوگرد بر روي هم تعيين شده است. توزيع عناصر الکتروپوزيتيو باقي مانده عمدتاً از روي واکنشهايي از نوع زير تعيين مي گردد:
M + Fe سيليکات Mسيليکات + Fe
M + Fe سولفيد Mسولفيد + Fe
بعبارت ديگر از روي انرژي آزاد سيليکاتها و سولفيدهاي مرتبط با سيليکاتها و سولفيدهاي آهن مي توان عوامل تعيين کننده توزيع عناصر در چنين سيستمي را پيش بيني کرد.
در قالب کلي عوامل تعيين کننده توزيع عناصر در يک چنين سيستمي را مي توان به صورت زير مجسم کنيم. آهن بخاطر فراواني بيش از اندازه اش در تمام فازهاي تقطير شده يعني دو فاز فلزي غني در الکترونهاي آزاد ، فاز يوني سيليکاته، و فاز احتمالاً کؤوالانت و نيمه فلزي سولفيدي حضور دارد. عناصري داراي الکتروپوزيتيويته بيش از آهن جايگزين آن در سيليکاتها شده و بدين ترتيب در سيليکاتها تجمع يافته اند. در مقابل عناصري که الکتروپوزيتيويته کمتري داشتند در فاز فلزي جمع شده و آهن در ترکيبات يوني جانشين آنها گرديد. فاز سولفيدي عناصري که اساساً با گوگرد ترکيبات تک قطبي تشکيل مي دادند و همچنين شبه فلزات و عناصري که نمي توانستند در مقادير قابل ملاحظه اي در محيطهاي يوني حضور داشته باشند را جذب مي کرد. اين عناصر در اصل فلزات گروه سولفيد شيمي تجزيه هستند.
توجه به اين نکته بسيار حائز اهميت است که توزيع عناصر در ميداني گرانشي مانند زمين نه از روي چگالي يا وزن اتمي (که طبيعتاً چنين انتظاري مي رود) بلکه از روي آفنيته آنها به فازهاي تشکيل شونده اصلي صورت مي گيرد. اين نيز به نوبه خود از روي آرايش الکتروني و بنابراين از روي مشخصات پيوند شيميايي اتمها کنترل مي شود. براي مثال ، اورانيوم و توريم اگر چه داراي چگالي بالايي هستند اما عناصري شديداً الکتروپوزيتيو بوده و بصورت اکسيد و سيليکات در پوسته زمين جمع شده اند. در مقابل فلزات طلا و پلاتين هيچ تمايلي به تشکيل سيليکات و اکسيد نداشته و بنابراين به آساني با آهن تشکيل آلياژ مي دهند. اين فلزات احتمالاً در هسته زمين تجمع يافته اند. توزيع عناصر مستقيماً از روي نيروي ثقل که صرفاً محل قرار گرفتن نسبي فازها را کنترل مي کند تعيين نمي شود، بلکه توزيع عناصر در اين فازها به پتانسيل شيميايي بستگي دارد.
طبقه بندي ژئوشيميايي عناصر: (Geochemical Classification Of Elimentes
گلدشميت (1923) اولين كسي بود كه به اهميت تفريق ژئوشيميايي اوليه عناصر (Primary Geochemical Diferentition) اشاره كرد اصطلاحات:
سيدروفيل = آهن دوست كالكوفيل = سولفيد دوست ليتوفيل = سيليكات دوست آتموفيل = اتمسفر دوست.
ماهيت ژئوشيميايي يك عنصر را مي توان با اندازه گيري توزيع آن بين سه فاز مايع- فلز، سولفيد و سيليكات تعيين كرد.
توزيع يك عنصر مشخص بين سه فاز فوق هنگامي عملي است كه اين سه فاز بطور مكانيكي از هم جدا شوند و جداگانه تجزيه گردند از روي چنين تجزيه هايي شركت پذيري هر عنصر بين فازهاي فلزي سيليكاتي و سولفيدي را به آساني مي توان محاسبه كرد. بعضي از عناصر به بيش از يك گروه گرايش نشان مي دهند زيرا توزيع هر عنصر تا حد زيادي به درجه حرارت فشار و كلاً محيط شيميايي سيستم بستگي دارد. اطلاعات بدست آمده از شخانه ها بوسيله اطلاعات حاصل از مطالعه فرآيند ذوب كوره ها مانند توزيع عناصر در ضمن ذوب كردن اسليت مس دار مانسفل در آلمان غربي تكميل گرديد. ذوب اين اسليت در كوره باعث تشكيل يك سرباره سيليكاتي و يك فاز غني از سولفيد آهن و مس و فاز آهن فلزي گرديد. اندازه گيريهاي انجام شده به روشهاي طيف نگاري در مورد غلظت بسياري از عناصر جزئي در فازهاي مختلف به تعيين ضرايب توزيعي منجر گرديده است كه مي توان گفت بطور كلي با ضرايب تعيين شده از روي مطالعات شخانه ها مطابقت دارد.
بر مبناي اين نتايج مي توان هر عنصر را بر اساس گرايش ژئوشيميايي آن به يكي از چهار گروه سيدروفيل، كالكوفيل، ليتوفيل و آتموفيل طبقه بندي كرد.
|
اتموفيل |
ليتوفيل |
کالکوفيل |
سيدروفيل |
|
(H) N (O) He Ne Ar Kr Xe |
Li Na K Rb Cs Be Mg Ca Sr Ba B Al Sc Y La-Lu Si Ti Zr Hf Th P V Nb Ta O Cr U H F Cl Br I (Fe) Mn (Zn) (Ga) |
(Cu) Ag Zn Cd Hg Ga In Ti (Ge) (Sn) Pb (As) (Sb) Bi S Se Te (Fe) Mo (Os) (Ru) (Rh) (Pd) |
Fe Co Ni Ru Rh Pd Os Ir Pt Au Rc Mo Ge Sn W C Cu Ga Ge As Sb |
عوامل مؤثر بر توزيع عناصر شيميايي:
بعضي از عناصر به بيش از يك گروه گرايش دارند زيرا توزيع هر عنصر شيميايي به عوامل زير بستگي دارند:
1- دما و فشار و بطور كلي محيط شيميايي سيستم
2- آرايش الكتروني اتمها
3- گرماي تشكيل
4- پتانسيل الكتروني
5- حجم اتمي
1) محيط شيميايي : كروميم در پوسته ليتوفيل اما اگر اكسيژن ناكافي باشد همچنان كه در بعضي از متئوريتها چنين است. كروميم قطعاً به گروه كالكوفيل تعلق دارد و منحصراً به سولفوراسپينل و دابروليت تبديل مي شود. بهمين ترتيب كربن و فسفر در محيط احيا ماهيتي سيدروفيل دارند.
2) آرايش الكتروني اتم ها: خواص ژئوشيميايي يك عنصر وسيعاً تحت تأثير آرايش الكتروني اتم هاي آن است و از اين رو به موقعيت سيستماتيك آن در جدول تناوبي بستگي دارد. مثلاً
عناصر ليتوفيل: عناصري هستند كه به آساني با آخرين پوسته 8 الكتروني خود يون مي سازند.
عناصر كالكوفيل: عناصر زير گروه B مي باشند كه يونهاي آن 18 الكترون در پوسته خارجي خود دارند.
عناصر سيدروفيل: عناصر زير گروه 8 و بعضي از عناصر مجاور آنهايند كه خارجي ترين پوسته الكتروني آنها اكثراً پر نشده است.
3) تفاوت در گرماي تشكيل: معياري براي سنجش خواص ليتوفيل است. اگر گرماي تشكيل يك اكسيد بيشتر از گرماي تشكيل FeO باشد عنصر ليتوفيل است به همين ترتيب عناصري كه اكسيد هايي با گرماي تشكيل كمتر از FeO دارند كالكوفيل يا سيدروفيلند.
4) پتانسيل الكتروني: اندازه گيري نيمه كمي عناصر ليتوفيل سيدروفيل يا عناصري كه خواص كالكوفيل دارند نيز توسط پتانسيل الكتروني امكان پذير است.
ليتوفيل : عناصري كه پتانسيل مثبت بالا دارند ( 1 تا 3 ولت) مثل فلزات قليايي و قليايي خاكي ليتوفيلند.
سيدروفيل: فلزات نجيب با پتانسيل منفي بالا سيدروفيل مي باشند.
كالكوفيل: عناصري كه در رديف واسطه قرار مي گيرند كالكوفيل مي باشند.
5) حجم اتمي : گلدشميت به همبستگي قابل توجه موجود بين ماهيت ژئوشيميايي و حجم اتمي اشاره كرد.
راهنمائي كلي در مورد ماهيت ژئوشيميايي عناصر:
1- مينرالوژي هر عنصر شايد نتواند بطور كامل نشان دهنده ماهيت ژئوشيميايي آن باشد. مثال : گرچه تمام كانيها تاليوم سولفيدي هستند اما بخش اعظم تاليوم پوسته اي زمين در درون شبكه كانيهاي پتاسيم قرار مي گيرد. بدين ترتيب كه يون Ti+ جايگزين يون K+ مي شود.
2- بطور كلي طبقه بندي هر عنصر به صورت ليتوفيل، كالكوفيل و يا سيدروفيل به رفتار آن در تعادلات مربوط به مايع – مايع در مذاب ها مربوط مي شود.
3- ماهيت ژئوشيميايي هر عنصر عمدتاً از روي آرايش الكتروني اتمهاي آن اراده شده بنابراين رابطه اي تنگاتنگ با عمل قرار گرفتن آن در جدول تناوبي دارد.